Akkumulator
Ein Akkumulator, kurz „Akku“ genannt, ist ein wieder aufladbarer Speicher für elektrische Energie auf elektrochemischer Basis. Ein Akku wird häufig auch als Batterie bezeichnet, wobei es sich bei dem Begriff auch um nicht wieder aufladbare Systeme handeln kann.
Ein Akku besteht aus einer oder mehreren galvanischen Zellen. In einer solchen Zelle findet eine Redoxreaktion statt: Reduktion und Oxidation laufen räumlich getrennt in je einer Halbzelle (Halbelement) an zwei Elektroden, die sich in einer Elektrolytlösung befinden, ab.
Es gibt verschiedene Akkutypen aus unterschiedlichen chemischen Substanzen mit jeweils unterschiedlichem Wirkungsgrad. Bekommt man z.B. aus einem Blei-Akku nur etwa 70% der zuvor gespeicherten Energie zurück, so sind es bei modernen Lithium-Ionen-Batterien, wie sie in Elektrofahrzeugen eingesetzt werden, nahezu 100%.
Man muss also grundsätzlich etwas mehr Energie in den Akku laden, als man später entnehmen kann.
Die verschiedenen Akkutypen unterscheiden sich durch das verwendete Elektrodenmaterial und den Elektrolyten. Elektrolyten können aus einer flüssigen Lösung, aus Gel oder auch einem Feststoff bestehen.
Beim Laden lässt man Strom durch den Akku fließen. Es wird eine chemische Reaktion ausgelöst, wodurch sich die Atome der beiden Elektroden verändern, sodass Sie eine Ladung aufweisen.
Welche Reaktionen sich einstellen, ist abhängig vom verwendeten
Akkutyp. Ab einem bestimmten Zustand ist nicht mehr genug ursprüngliches Elektrodenmaterial für diese Reaktion vorhanden.
Der Akku darf dann nicht weiter geladen werden, da sich sonst unerwünschte chemische Reaktionen einstellen, die zur Zerstörung führen
können.
Um dies zu verhindern, werden die Ladeeinrichtungen überwiegend mit elektrotechnischem Überladungsschutz versehen. In Elektrofahrzeugen wird der Schutz gegen Überladung des Akkus durch ein intelligentes Batteriemanagement sichergestellt.
Bei der Entnahme der gespeicherten Energie kehrt sich der oben geschilderte Prozess um.
Strom kann solange entnommen werden, bis keine Reaktion mehr stattfinden kann, da die Reaktionspartner aufgebraucht sind.
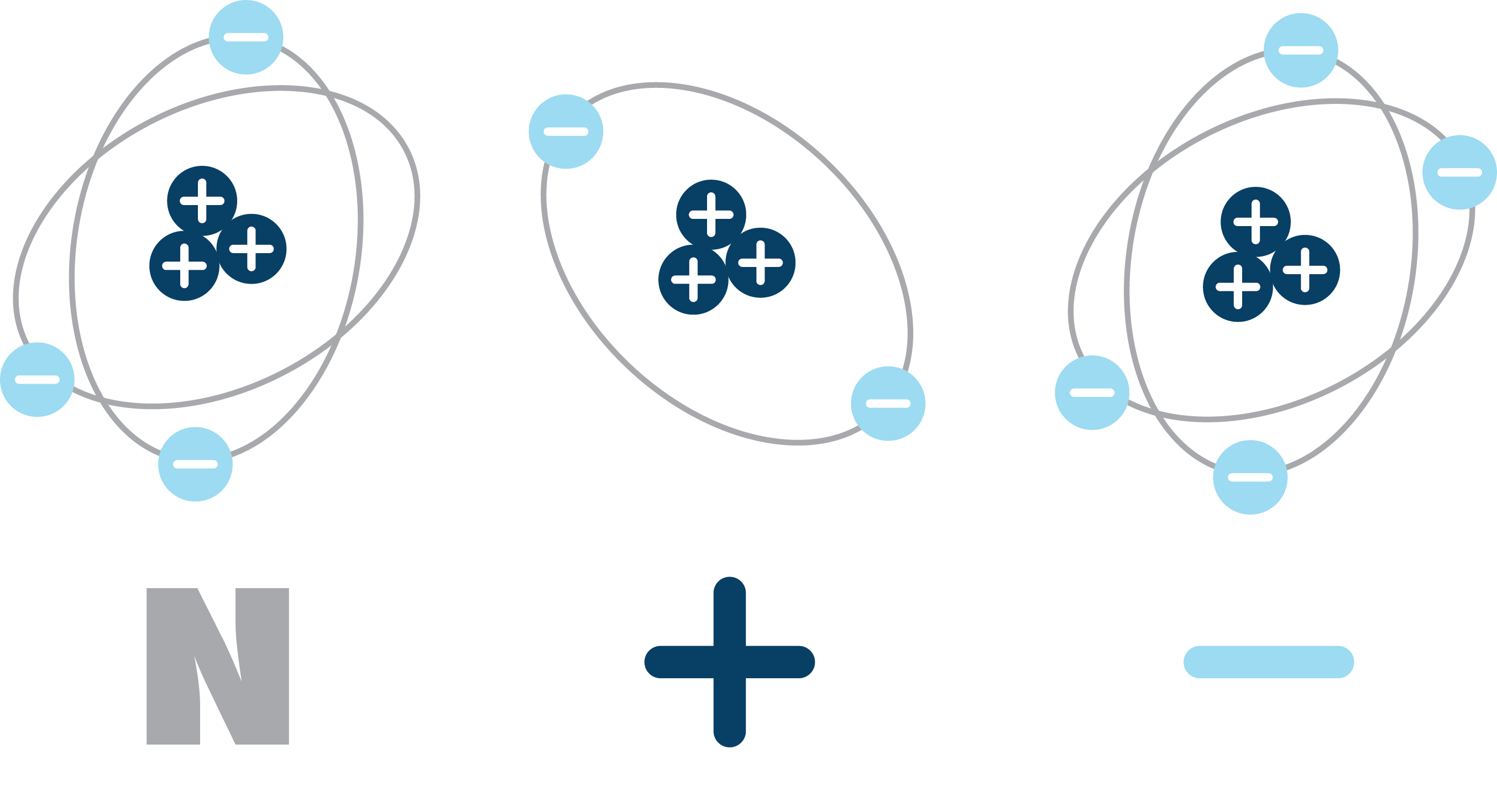
Abbildung 4: Schematische Darstellung der Ladung von Atomen
